Імуногенетика — це наука на стику генетики та імунології, яка вивчає, як наші гени визначають силу і точність захисних реакцій організму. Вона пояснює, чому один і той самий вірус для когось стає легкою застудою, а для іншого — важкою хворобою, чому пересаджені органи іноді приживаються, а іноді відторгаються з нищівною силою. Гени не просто передають колір очей чи форму носа — вони диригують цілим оркестром клітин, антитіл і рецепторів, які щосекунди розпізнають «своє» від «чужого».
У генетичному ключі імунітет постає як система охорони внутрішньої стабільності, здатна миттєво реагувати на будь-яку загрозу, несучи ознаки чужорідної інформації. Ця дисципліна розкриває закономірності успадкування антигенної специфічності та роль генетичних механізмів у кожній імунній реакції. Для початківців це як ключ до розуміння, чому в родині хтось постійно хворіє на аутоімунні захворювання, а хтось — ні. Для просунутих читачів — це глибоке занурення в поліморфізм генів, рекомбінацію сегментів і сучасні технології, які вже сьогодні рятують життя під час трансплантацій чи персоналізованої терапії.
Сьогодні імуногенетика виходить далеко за межі лабораторій. Вона допомагає прогнозувати ризики хвороб, підбирати ідеальних донорів органів і навіть створювати нові ліки, що враховують індивідуальний генетичний профіль. Гени імунної системи — це не статична карта, а живий, динамічний код, що постійно еволюціонує разом з нами.
Історія розвитку імуногенетики: від перших відкриттів крові до геномної ери
Усе почалося на початку XX століття, коли Карл Ландштейнер у 1901 році відкрив систему груп крові АВО. Це стало першим реальним доказом, що антигени на поверхні клітин передаються у спадок. Люди раптом зрозуміли: несумісність крові — не випадковість, а генетична закономірність. Пізніше Пол Наттом порівняв білки сироватки крові людини і мавп, заклавши основу серологічного вивчення антигенів.
У 1930–1940-х роках науковці зосередилися на гістосумісності — причинах, чому пересаджені тканини відторгаються. Відкриття комплексів генів, що кодують поверхневі молекули на клітинах, стало справжнім проривом. Саме тоді зародилася ідея, що імунітет — це не просто реакція на інфекцію, а глибоко генетично запрограмована система розпізнавання «чужого».
1960-ті роки принесли розуміння геномної організації імуноглобулінів. Вчені з’ясували, як один і той самий ген може створювати мільйони варіантів антитіл. Паралельно досліджували генетичний контроль сили імунної відповіді — чому одні люди виробляють потужні антитіла, а інші — слабкі. Усе це злилося в чотири ключові напрями імуногенетики: генетика гістосумісності, організація генів антитіл, контроль імунної відповіді та вивчення антигенів клітин і тканин.
Сьогодні, у 2025–2026 роках, імуногенетика переживає справжній ренесанс завдяки технологіям секвенування нового покоління (NGS). Поліморфізм генів HLA сягає десятків тисяч алелів, і наука вже вміє їх швидко розшифровувати для точного підбору терапії.
Основні поняття імуногенетики: антигени, антитіла та генетичний контроль
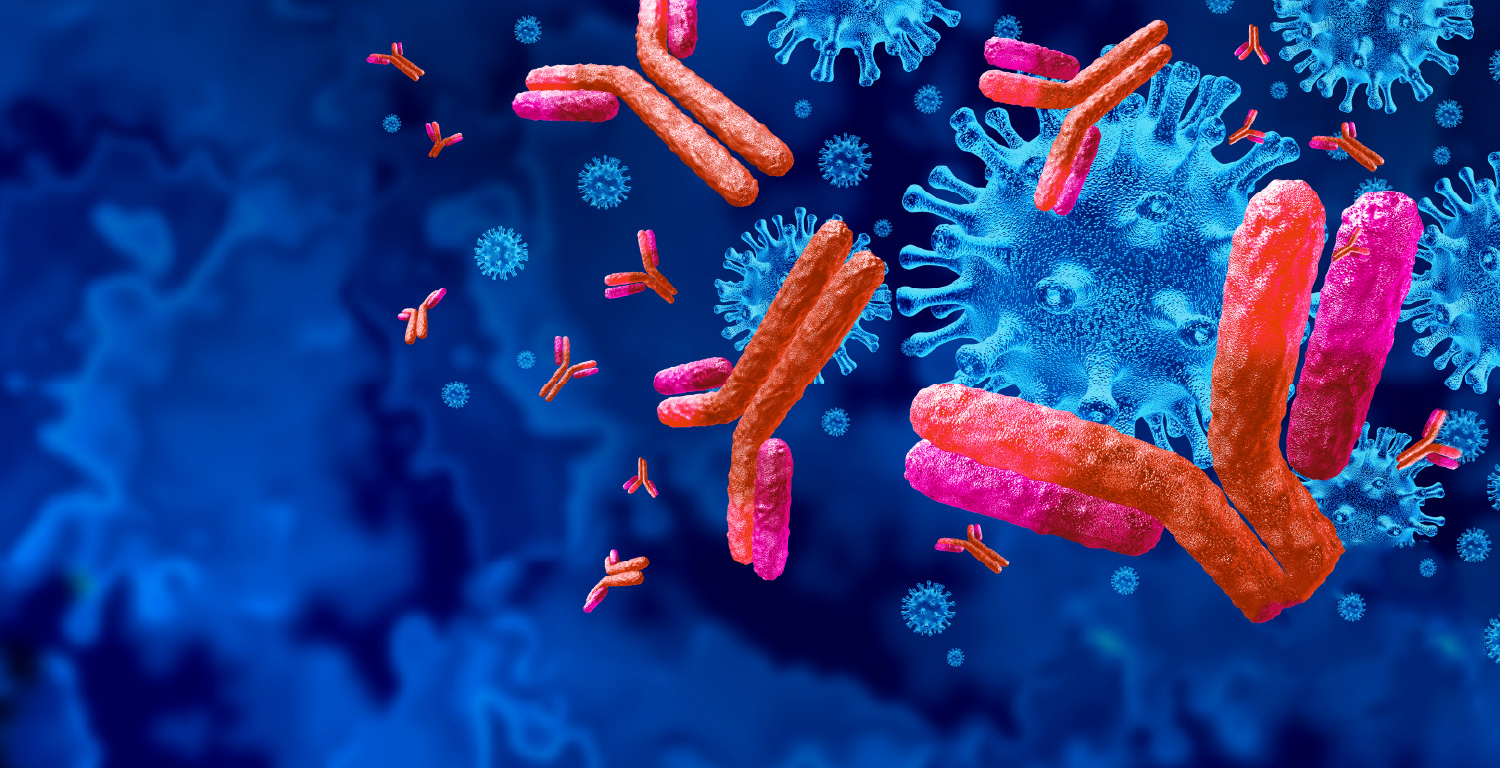
Антигени — це маркери на поверхні клітин, вірусів чи бактерій, які імунна система розпізнає як «чужі». Вони можуть бути повними (з білковою частиною) або неповними (гаптенами). Епітопи, або антигенні детермінанти, — це саме ті маленькі ділянки, до яких точно «прилипають» антитіла. Суперантигени, як у деяких бактерій, здатні викликати масову активацію лімфоцитів, що призводить до цитокінового шторму.
Антитіла, або імуноглобуліни, — це білки, які нейтралізують загрозу. Вони мають Y-подібну форму з двома важкими і двома легкими ланцюгами. Кожен клас імуноглобулінів (IgM, IgG, IgA, IgE, IgD) виконує свою роль: IgM — перша лінія оборони, IgG — довгостроковий захист, IgA — охорона слизових. Але справжня магія відбувається на рівні генів.
Генетичний контроль імунної відповіді включає гени Ir (immune response), які визначають, наскільки сильно організм відреагує на конкретний антиген. У людей ці гени тісно пов’язані з головним комплексом гістосумісності.
Головний комплекс гістосумісності (HLA): серце і ключ до сумісності
HLA — це людський аналог MHC (major histocompatibility complex), розташований на 6-й хромосомі. Він складається з трьох класів генів. Клас I (HLA-A, B, C) представляє антигени всередині клітини на поверхні — ідеально для розпізнавання вірусів і пухлин Т-кілерами. Клас II (HLA-DR, DP, DQ) працює на антиген-презентуючих клітинах і активує Т-хелперів. Клас III кодує компоненти комплементу та інші молекули запалення.
Поліморфізм HLA вражає: станом на 2025 рік відомо понад 43 тисячі алелів тільки для HLA-генів. Кожна людина має унікальну комбінацію — справжній генетичний «відбиток» імунітету. Саме через це пересадка органів вимагає ретельного HLA-типування. Несумісність призводить до відторгення, а ідеальна — до довгого життя трансплантата.
У практиці HLA-асоціації з хворобами вражають. HLA-B27 зустрічається у 90% пацієнтів з анкілозуючим спондилітом. HLA-DQ2 і DQ8 — у більшості хворих на целіакію. Такі зв’язки дозволяють прогнозувати ризики ще до появи симптомів.
| HLA-алель | Асоційоване захворювання | Частота асоціації |
|---|---|---|
| HLA-B27 | Анкілозуючий спондиліт | до 90% |
| HLA-DQ2/DQ8 | Целіакія | понад 95% |
| HLA-DR4 | Ревматоїдний артрит | близько 70% |
| HLA-B57 | Гіперчутливість до абакавіру | понад 90% |
Джерело даних: Фармацевтична енциклопедія та міжнародні бази IPD-IMGT/HLA.
Гени імуноглобулінів: як один ген створює мільйони варіантів
Різноманітність антитіл забезпечує V(D)J-рекомбінація — унікальний процес, що відбувається тільки в лімфоцитах. Сегменти V (variable), D (diversity) і J (joining) перемішуються в майже випадковому порядку. Додаються джанкціональні мутації та соматичні гіпермутації після зустрічі з антигеном. Результат? Понад 10^12 можливих варіантів рецепторів — більше, ніж зірок у Чумацькому Шляху.
Гени імуноглобулінів розташовані в кількох локусах: для важких ланцюгів на 14-й хромосомі, для легких κ — на 2-й, λ — на 22-й. Кожен ланцюг кодується щонайменше двома генами: V для специфічності і C для класу. Під час дозрівання В-клітин відбувається реаранжировка — генетичний «шаховий матч», який створює унікальний рецептор.
Цей механізм пояснює, чому імунітет може реагувати на будь-яку нову загрозу, навіть якщо раніше такого антигену не існувало. Еволюція подарувала нам цю генетичну гнучкість, і імуногенетика допомагає зрозуміти, коли вона дає збій — наприклад, при первинних імунодефіцитах.
Зв’язок імуногенетики з захворюваннями та персоналізованою медициною
Генетичні варіанти HLA визначають не тільки сумісність тканин, але й сприйнятливість до інфекцій, аутоімунних хвороб і навіть реакцій на ліки. Наприклад, носії певних алелів HLA-B*57:01 мають високий ризик важкої реакції на препарат абакавір, що використовується при ВІЛ. Тестування перед призначенням — стандарт у сучасній практиці.
У трансплантології імуногенетика — це запорука успіху. Точне високорозділене типування HLA за допомогою NGS дозволяє підбирати донорів з мінімальним ризиком відторгнення. У репродуктивній медицині вивчення імуногенетичних факторів допомагає пояснити повторні викидні через несумісність материнського і плідного HLA.
Персоналізована імунотерапія раку також спирається на імуногенетику. CAR-T-клітини, що редагуються за допомогою CRISPR, часто вимагають модифікації HLA, щоб уникнути відторгнення. Нові дослідження 2025–2026 років активно тестують «універсальні» Т-клітини без поверхневих HLA-молекул.
Практичні кейси імуногенетики в сучасній медицині
Кейс 1. Трансплантація нирки. Пацієнтка з термінальною нирковою недостатністю мала рідкісний HLA-фенотип. Завдяки національному реєстру донорів і високоточному NGS-типуванню вдалося знайти ідеально сумісного донора. Результат — успішна пересадка без довічного високодозового імуносупресії.
Кейс 2. Целіакія в дитини. Генетичний тест виявив HLA-DQ2.8. Рання дієта без глютену запобігла розвитку хвороби, хоча симптоми ще не проявилися.
Кейс 3. ВІЛ-терапія. Перед призначенням абакавіру провели скринінг на HLA-B*57:01. Позитивний результат — препарат замінили, уникнувши небезпечної реакції.
Ці приклади показують, як імуногенетика переходить від теорії до щоденної практики, рятуючи життя і покращуючи якість лікування.
Сучасні тренди та майбутнє імуногенетики
Секвенування нового покоління зробило HLA-типування швидким і доступним. Штучний інтелект прогнозує імунну відповідь на вакцини ще до клінічних випробувань. CRISPR-Cas9 дозволяє редагувати гени імунної системи безпосередньо в пацієнта — від лікування первинних імунодефіцитів до створення стійких до ВІЛ клітин.
У популяційній імуногенетиці вивчають, як міграції народів формували різноманіття HLA. В Україні активно розвиваються центри генетичної діагностики, де проводять імуногенетичні дослідження для дітей з імунодефіцитами та онкологією.
Імуногенетика вже сьогодні дає інструменти для профілактики. Генетичний паспорт імунітету може стати таким же звичайним, як аналіз крові. Вона знімає завісу з того, чому одні люди живуть до ста років без серйозних хвороб, а інші — борються з хронічними запаленнями все життя.
Кожного дня нові відкриття додають деталі до цієї генетичної картини захисту. Імуногенетика не просто пояснює, чому ми хворіємо — вона показує, як зробити так, щоб хворіти менше. І в цьому її справжня сила для кожного з нас.












Залишити відповідь