Електроліз розкриває таємниці матерії, ніби чарівник, що розкладає воду на кисень і водень за допомогою невидимої сили струму. Цей процес, відкритий понад два століття тому, перетворює звичайні речовини на чисті елементи, ніби розплутуючи вузли в хімічному клубку. Уявіть, як постійний електричний струм пронизує розчин або розплав, змушуючи іони танцювати до електродів, де відбуваються справжні перетворення – окиснення і відновлення, що змінюють усе навколо.
Суть електролізу ховається в електрохімічних реакціях, де струм стає каталізатором розкладу. Позитивно заряджені катіони мандрують до катода, набираючи електрони, а негативні аніони спрямовуються до анода, віддаючи їх. Ця динаміка не просто теорія – вона живе в лабораторіях і заводах, де електроліз витягує метали з руд чи очищає воду від домішок. Згадуючи перші експерименти, не можна не відзначити, як вони революціонізували розуміння електрики та хімії, зробивши неможливе реальним.
Історія відкриття електролізу: від перших іскор до сучасних відкриттів
У 1800 році Алессандро Вольта створив першу батарею, що стала ключем до електролізу, ніби відкривши двері в новий світ. Невдовзі, у тому ж році, англійські вчені Вільям Ніколсон і Ентоні Карлайл розклали воду на водень і кисень, спостерігаючи, як бульбашки газу піднімаються з електродів наче з глибин океану. Цей момент став переломним, адже показав, що електрика може розщеплювати молекули, розкриваючи їхню приховану природу.
Майкл Фарадей, геній електрохімії, у 1830-х роках сформулював закони електролізу, які й досі є основою. Він виявив, що кількість речовини, яка виділяється, пропорційна заряду, що пройшов через електроліт – проста, але потужна ідея, ніби математичний компас у хаосі реакцій. Ці відкриття поширилися по світу, надихаючи промислові революції, від видобутку алюмінію до створення синтетичних матеріалів. Сьогодні, у 2025 році, електроліз еволюціонує з використанням відновлюваної енергії, роблячи його екологічним героєм у боротьбі з кліматичними змінами.
Не забуваймо про внесок українських вчених, як-от ті, хто в радянські часи розвивали електроліз для металургії. Їхні роботи, описані в архівах, показують, як локальні інновації вплинули на глобальну науку, додаючи шар культурної глибини до цієї історії.
Основні принципи електролізу: як це працює на молекулярному рівні
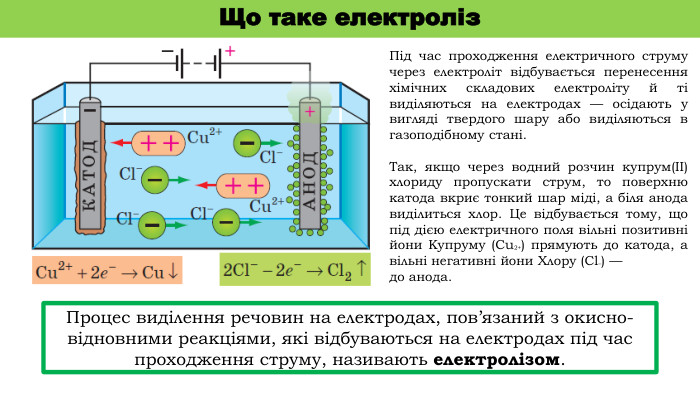
Уявіть електроліз як симфонію, де електроди – диригенти, а іони – музиканти. Коли постійний струм проходить через електроліт – розчин або розплав солі, кислоти чи лугу – позитивні іони (катіони) притягуються до негативного катода. Там вони набирають електрони, відновлюючись, наприклад, перетворюючи іони міді на чистий метал, що осідає шаром, ніби іній на вікні.
З іншого боку, негативні аніони рухаються до позитивного анода, де віддають електрони, окиснюючись. У водному розчині це може призвести до виділення кисню або хлору, залежно від речовини. Фарадеївські закони уточнюють: маса виділеної речовини дорівнює M = (Q / F) * (1 / z), де Q – заряд, F – константа Фарадея (приблизно 96 485 Кл/моль), z – кількість електронів. Ця формула, перевірена в численних експериментах, робить процес передбачуваним і точним.
Для просунутих: розгляньмо потенціали електродів. Стандартний потенціал визначає, яка реакція переважатиме – наприклад, у електролізі води з сульфатом натрію на інертних електродах виділяється водень на катоді (E° = -0.83 В) і кисень на аноді (E° = 1.23 В). Але в реальності потрібна надпотенціал, щоб подолати бар’єри, роблячи процес ефективнішим з каталізаторами.
Різновиди електролізу: від розплавів до розчинів
Електроліз розплавів, як у виробництві натрію з хлориду натрію, відбувається при високих температурах, де іони вільно рухаються без води. Це ніби танець у розпеченій лаві, де на катоді осідає метал, а на аноді – газ. У водних розчинах усе складніше через конкуренцію з водою, де на катоді може виділятися водень замість металу, якщо потенціал не підходить.
Мембранний електроліз додає сучасний поворот, використовуючи перегородки для розділення продуктів, як у виробництві хлору та лугу. Ці варіанти роблять електроліз гнучким інструментом, адаптованим до різних потреб.
Застосування електролізу в науці: лабораторні дива та відкриття
У наукових лабораторіях електроліз стає інструментом для синтезу, ніби алхімік, що створює нові сполуки. Він допомагає вивчати ізотопи, розділяючи їх за масою, або аналізувати розчини через кількість виділеного газу. У біохімії електроліз використовують для очищення білків, де струм змушує молекули мігрувати, ніби в уповільненому танці.
Сучасні дослідження, станом на 2025 рік, фокусуються на електролізі для зберігання енергії, перетворюючи надлишок сонячної електрики на водень. Це не просто теорія – проекти в Європі вже виробляють “зелений” водень, зменшуючи залежність від викопного палива.
Промислові застосування електролізу: від металів до екології
У промисловості електроліз – це робоча конячка, що витягує алюміній з бокситів у процесі Холла-Еру, де розплавлений криоліт стає електролітом при 950°C. Щорічно виробляється мільйони тонн металу, роблячи його доступним для авіації та упаковки. Аналогічно, електроліз виробляє мідь, цинк і навіть золото, очищаючи їх до блиску.
У екологічній сфері електроліз очищає стічні води, розкладаючи забруднювачі, або генерує хлор для дезінфекції. У 2025 році, з ростом відновлюваної енергії, електроліз стає ключем до водневої економіки, де водень з води стає паливом майбутнього, зменшуючи викиди CO2.
Ось порівняння ключових промислових процесів:
| Процес | Електроліт | Продукти | Застосування |
|---|---|---|---|
| Електроліз води | Кислотний розчин | Водень, кисень | Паливо, зварювання |
| Виробництво алюмінію | Розплавлений криоліт | Алюміній, кисень | Металургія |
| Хлор-лужний процес | Розчин NaCl | Хлор, NaOH, водень | Хімія, очищення |
Ці дані базуються на інформації з сайтів як uk.wikipedia.org та pharmencyclopedia.com.ua. Таблиця ілюструє різноманітність, показуючи, як електроліз адаптується до потреб.
Переваги та виклики електролізу: баланс сили та обмежень
Електроліз пропонує чисті продукти без забруднюючих реагентів, ніби зелений чарівник у світі хімії. Він ефективний для високоточних процесів, як гальванопластика, де метали наносяться шаром за шаром, створюючи ювелірні вироби чи електроніку. Екологічна перевага – у виробництві водню без викидів, що робить його союзником у переході до стійкої енергетики.
Однак виклики існують: висока енергоспоживання, корозія електродів і потреба в чистому електроліті. У 2025 році інновації, як нано-каталізатори, зменшують ці проблеми, роблячи процес дешевшим і ефективнішим.
Цікаві факти про електроліз
- 🔥 Перший електроліз води призвів до вибуху, коли вчені змішали гази – урок про обережність у науці!
- ⚡ Константа Фарадея дорівнює заряду одного моля електронів, що робить її універсальною для розрахунків у всьому світі.
- 🌍 У 2025 році електроліз виробляє понад 5% світового водню, з планами на 20% до 2030 року, за даними енергетичних агентств.
- 🧪 Електроліз використовують у косметиці для створення іонізованої води, яка нібито краще зволожує шкіру – суміш науки та маркетингу.
- 🚀 НАСА застосовує електроліз для генерації кисню на Міжнародній космічній станції, роблячи космос ближчим.
Ці факти додають шар чарівності, показуючи, як електроліз пронизує повсякденне життя, від лабораторій до зірок. Для початківців це надихає експериментувати вдома з простими установками, а просунуті можуть заглибитися в квантові аспекти реакцій.
Майбутнє електролізу: інновації та перспективи
У 2025 році електроліз еволюціонує з появою фотоелектрохімічних клітин, де сонячне світло безпосередньо розкладає воду, ніби природа сама стає інженером. Дослідження фокусуються на ефективності, досягаючи 20% конверсії енергії, що робить його конкурентним з традиційними методами. Уявіть міста, де водневі станції працюють на сонці, живлячи автомобілі без краплі бензину.
Виклики, як вартість електродів з платини, вирішуються альтернативами на основі заліза чи вуглецю. Це відкриває двері для глобального поширення, особливо в країнах з великим потенціалом відновлюваної енергії, як Україна з її сонячними полями.
Електроліз не стоїть на місці – він пульсує з ритмом прогресу, обіцяючи світ, де енергія чиста, а хімія – союзник людства. Кожен новий крок робить його ближчим до повсякденності, ніби невидима сила, що формує завтра.











Залишити відповідь