Водень — це найпростіший хімічний елемент із атомним номером 1, символом H, який у формі молекули H₂ утворює безбарвний, без запаху газ, найлегший серед усіх відомих речовин. Його густина при стандартних умовах ледь досягає 0,09 г/л, роблячи його в 14,4 раза легшим за повітря, ніби невагома пір’їнка, що мріє втекти в небо. Цей газ становить близько 75% маси баріонної матерії Всесвіту, ховаючись у зорях, планетах і навіть у воді, без якої немає життя.
Уявіть потік цього невидимого енергоносія: водень згорає з вибухом у суміші з киснем, але продукує лише пару — чисту воду. На Землі його добувають промислово сотнями мільйонів тонн щороку, переважно з природного газу, але мрія про “зелений” водень набирає обертів, обіцяючи революцію в енергетиці. Від шкільних реакцій цинку з кислотою до паливних елементів у Toyota Mirai — водень всюди пронизує нашу реальність.
Його відкрив Генрі Кавендіш у 1766 році, реагуючи метали з кислотами, а назву “гідроген” — “той, що породжує воду” — дав Антуан Лавуазьє. Сьогодні, у 2026-му, водень не просто елемент підручника: це паливо майбутнього, яке ЄС планує виробляти на 20 мільйонів тонн до 2030-го, замінюючи газ і вугілля (uk.wikipedia.org).
Будова атома водню: простота, що ховає силу
Атом водню — еталон мінімалізму в хімії: одне протон у ядрі та один електрон на орбіталі. Без нейтронів у базовій формі протію, цей “голий” протон визначає його унікальність. Електронна конфігурація 1s¹ робить водень мостом між металами та неметалами — іноді він поводиться як лужний метал, утворюючи гідриди з Na чи Ca, а інколи як галоген, реагуючи з киснем.
Але справжня магія — в ізотопах, де різниця в масі нейтронів кардинально змінює властивості. Водень не стоїть на місці: у зірках він зливається в гелій, вивільняючи енергію Сонця. На Землі його атомна маса 1,00794 а.о.у., що робить його найлегшим елементом таблиці Менделєєва.
Ця простота обманює: водень проникає крізь метали, викликаючи крихкість, і вбудовується в білки, ДНК, воду — основу всього живого. Без нього не було б океанів чи атмосфери, як ми їх знаємо.
Фізичні властивості водню: легкість і крихкість
При кімнатній температурі водень — газ, що злітає вгору швидше за гелій, бо його молекули носяться з шаленою швидкістю 1920 м/с. Температура кипіння мінус 252,87°C, плавлення — мінус 259,16°C, роблячи рідкий водень ідеальним охолоджувачем для ракетних двигунів NASA. Він погано розчиняється у воді — лише 0,018 об’ємів на об’єм при 20°C, але чудово дифундує через сталі, викликаючи ефекти типу “водневе ламання”.
Теплота згоряння H₂ сягає 286 кДж/моль — найвища серед палив, з енергоефективністю 120-142 МДж/кг. Рідкий водень має щільність 70,8 кг/м³, але вимагає криогенних умов, що ускладнює зберігання. Його дифузійність робить водень “привидом” матеріалів — він просочується крізь пластини товщиною в міліметр за години.
Ці властивості роблять його небезпечним: суміш 4-75% H₂ з повітрям вибухова. Але в балонах чи трубах, з правильними клапанами, він слухняний слуга промисловості.
Хімічні властивості водню: від спокою до бурі
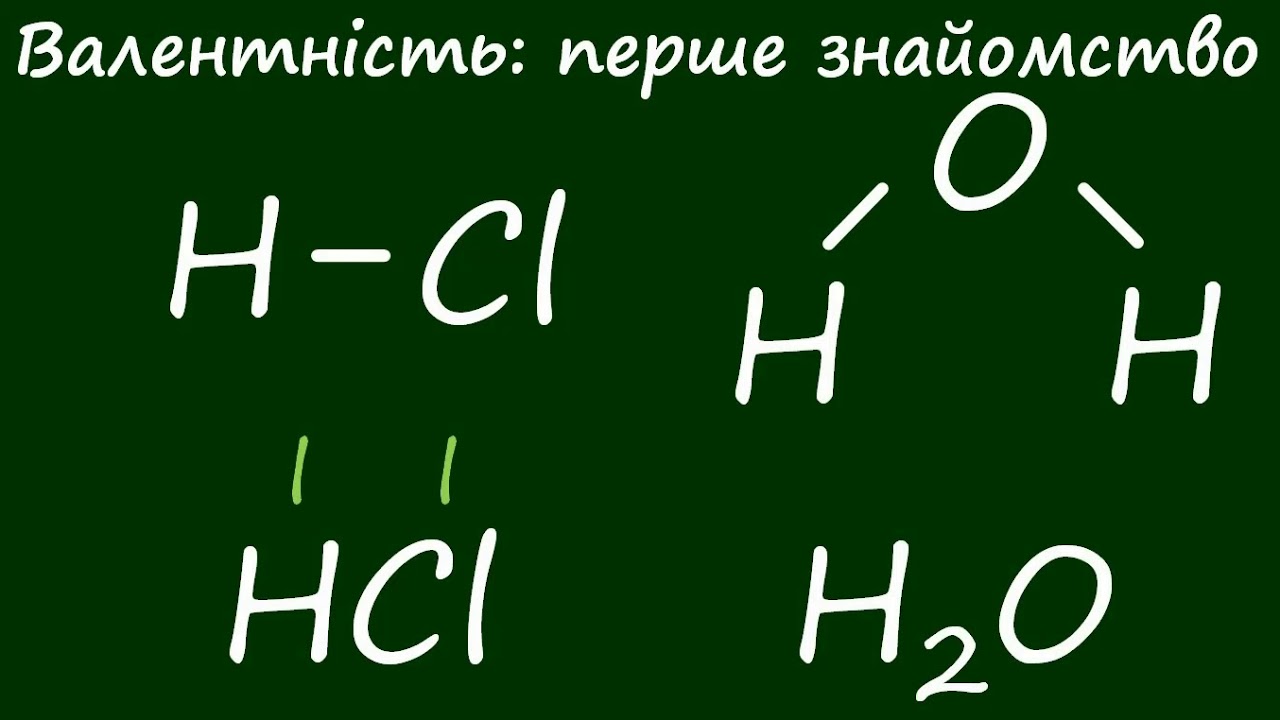
Водень малореактивний за кімнати, але нагрійте — і він оживає. З киснем утворює “гримучий газ”, що вибухає з енергією 2420 кДж/м³, як у дирижаблі “Гінденбург” 1937-го. З хлором на світлі — HCl, з фтором — миттєвий вибух. Метали типу Li, Na дають іонні гідриди MHₓ, що реагують з водою: NaH + H₂O → NaOH + H₂.
Він відновник: з CuO при нагріванні дає мідь і воду, гідрує ненасичені олії в маргарин. У кислотах чи лугах поводиться амфотерно. Ця двоїстість робить водень універсалом реакцій.
У плазмі чи зірках — термоядерний синтез: 4H → He + енергія. Земні реактори поки мріють про це, але ITER у Франції наближається.
Ізотопи водню: різні обличчя одного елемента
Водень має три стабільні форми: протій ¹H без нейтронів, дейтерій ²H з одним, тритій ³H з двома (радіоактивний, період напіврозпаду 12,32 роки). Протій — 99,98% природного водню, дейтерій — 0,0156%, зосереджений у “важкій воді” D₂O для ядерних реакторів. Тритій синтезують, використовуючи в термоядерних бомбах чи маяках.
Властивості різняться: важка вода кипить при 101,4°C, дейтерій реагує повільніше через більшу масу. У біології дейтерій токсичний у високих дозах, порушуючи ферменти.
| Ізотоп | Символ | Масова частка | Період напіврозпаду | Застосування |
|---|---|---|---|---|
| Протій | ¹H | 99,98% | Стабільний | Універсальне |
| Дейтерій | ²H (D) | 0,0156% | Стабільний | Ядерні реактори, NMR |
| Тритій | ³H (T) | Сліди | 12,32 роки | Термоядерна енергія |
Джерела даних: uk.wikipedia.org, pharmencyclopedia.com.ua. Ця таблиця показує, як мала зміна в ядрі змінює все — від стабільності до реактивності.
Як отримують водень: від пробірки до гігантських заводів
У лабораторії все просто: активні метали на кислотах, як Zn + 2HCl → ZnCl₂ + H₂↑, або алюміній з лугом. Газ збирають “під водою” через легкість. Але промисловість — інша справа: 96% водню з парової конверсії метану CH₄ + H₂O → CO + 3H₂ при 800°C з Ni-каталізатором, потім shift-реакція CO + H₂O → CO₂ + H₂.
Електроліз води — 2H₂O → 2H₂ + O₂ — класичний, але енерговитратний (50-60 кВт·год/кг). “Зелений” варіант на сонячних чи вітрових електростанціях набирає ходу. Газифікація вугілля C + H₂O → CO + H₂ дає “чорний” водень.
У 2025-2026 глобальне виробництво сягає 120 млн тонн/рік, з них лише 4% зелений. Витрати: сірий — 1-2 $/кг, зелений — 3-6 $/кг, але падають з дешевою ВДЕ.
- Парова конверсія: Найдешевша, але CO₂-інтенсивна, домінує в Азії.
- Електроліз PEM/алкалічний: Ефективний для зелених джерел, масштабується.
- Піроліз метану: Перспективний, без CO₂, але поки пілотний.
Після списку: Ці методи еволюціонують — Китай будує гігафабрики PEM на 1 ГВт, Європа субсидує CCS для блакитного. Україна планує експорт 0,5-2 млн т/рік до 2030 (hydrogen.ua).
Типи водню за “кольорами”: сірий, блакитний, зелений
| Тип | Метод виробництва | Викиди CO₂ (кг/кг H₂) | Частка ринку (%) |
|---|---|---|---|
| Сірий | Reforming CH₄ без CCS | 9-12 | 96 |
| Блакитний | Reforming + CCS | 1-2 | <1 |
| Зелений | Електроліз ВДЕ | 0 | 4 |
Джерела: uk.wikipedia.org, IRENA.org. Зелений водень — зірка 2026-го, з планами ЄС на 42% заміни сірого до 2030-го. Ці кольори визначають екологічність: сірий годує промисловість, але душить клімат, зелений — чисте майбутнє.
Застосування водню: від добрив до космічних польотів
Половину світового водню “з’їдає” синтез аміаку за Габером-Бошем: N₂ + 3H₂ → 2NH₃, основа 180 млн т добрив щороку. Нафтопереробка гідрує фракції, видаляючи сірку. Гідрогенізація олій дає маргарин, метанол — паливо та пластмаси.
- Промислове зварювання: H₂ + O₂ у факелі до 3000°C.
- Харчова галузь: перетворення рослинних олій на тверді жири.
- Медицина: дейтерій у МРТ-контрастах.
Після списку: Водень скрізь — від скла (відновник) до електроніки (епітаксія GaN). У 2026-му його споживання росте на 5-7% щороку, з фокусом на декарбонізацію.
Водень як паливо майбутнього: енергетична революція 2026
Паливні елементи перетворюють H₂ + ½O₂ → H₂O + 0,5 МВт·год/кг — удвічі ефективніше бензину. Toyota Mirai проїжджає 650 км на 5 кг, Hyundai Nexo — вантажівки. У Європі 40 тис. FCV на дорогах, плани на 7 млн до 2030.
Енергетика: PEM-електrolізери на вітряках виробляють H₂ для зберігання надлишків. ЄС REPowerEU: 10 Mt prod + 10 Mt imp. Україна — стратегія до 2050, пілоти на “ДТЕК” та “Нафтогаз”, експорт через Словаччину. Глобальні інвестиції в H₂ — 8 млрд $ у 2025, +70% росту.
Транспорт: судна на H₂ (MAN Energy), літаки Airbus ZEROe. Пром: ArcelorMittal тестує H₂-відновлення заліза замість коксу. Ризики? Вибухонебезпека, але сенсори та норми тримають у шорах.
Роль водню в природі, біології та космосі
У біології водень — половина атомів у воді, органічних молекулах. Ферменти як гідрогеназа в бактеріях виробляють H₂ метаболічно. У космосі — 88% атомів, паливо Великого Вибуху, протон-протонний цикл у Сонці: 4¹H → ⁴He + енергія.
На Юпітері — 90% атмосфери H₂, комети несуть його з льодом. Життя? Метаногени на Землі живуть на H₂+CO₂. У 2026 NASA шукає H₂ на Європі як біомаркер.
Природа циклічна: фото синтез фіксує H у вуглеводи, вулкани викидають H₂S. Водень пов’язує все — від клітин до галактик.
Цікаві факти про водень
Водень — єдиний елемент, синтезований у Великому Вибуху в значних кількостях, решта — зірковий “альхімік”.
У дирижаблях 1930-х H₂ підіймав “Гінденбург”, але вибух через статичну іскру став уроком історії.
Найвища теплота пароутворення серед газів — 0,904 кДж/г, чому ракети Space Shuttle пили тонни рідкого H₂.
Дейтерій у океанах — 33 г/т, достатньо для мільйонів ядерних реакторів.
Ви не повірите: H₂ у водневій воді обіцяють антиоксидантний ефект, хоч докази суперечливі (pharmencyclopedia.com.ua).
Ці перлини роблять водень не просто газом — легендою науки. Його шлях від лабораторії Кавендіша до водневих хабів Європи тільки починається, обіцяючи чисту енергію для поколінь.













Залишити відповідь